臨床研究 CLINICAL RESEARCH
プロバイオティクス
犬の慢性腸症に対する
プロバイオティクスの
効果に関する研究
概要
当院にて慢性腸症と診断された犬に対し、標準治療+プロバイオティクス、標準治療+プラセボの二群に分け、臨床症状、腸内細菌叢などについて評価します。
背景・目的
犬の慢性腸症は頻繁に遭遇する慢性消化管疾患であり、食事療法、プレドニゾロンなどで治療されてきました。近年、腸内細菌叢と慢性腸症の関連性が注目されており、腸内細菌叢により積極的に介入することの重要性が示唆されています。海外にはVivomixxやVSL#3といった犬の慢性腸症に対して有効なプロバイオティクスが販売されていますが、日本国内で利用可能なプロバイオティクスでは、犬の慢性腸症に対する有効性は証明されていません。
Sivomixxは先述のプロバイオティクスと類似した菌種、菌数を有する国内で入手可能なプロバイオティクスであり、犬の慢性腸症に対する有効性が期待されています。本研究では、犬の慢性腸症に対するSivomixxの有効性に関し、プラセボを用いた比較臨床研究によって多角的に検討することを目的としています。
対象
当院にて各種スクリーニング検査にて慢性腸症と診断された犬
除外基準
- 内視鏡検査によって消化器型リンパ腫など、他の疾患であると診断された犬
- 担当医によって研究の継続が不適切であると判断された犬

内容
- 通常の手順にて慢性腸症と診断された犬
- 低アレルゲン食、プレドニゾロンを用いた標準治療を開始
- Sivomixx群、プラセボ群に無作為に振り分けて上記治療と合わせて投与
- 臨床症状、血液検査などを3ヶ月後までモニタリング
- 初診時、最終評価日に血液、糞便を採取し、糞便のメタゲノム、短鎖脂肪酸などを解析
- 研究にご協力いただいた場合、プロバイオティクスは無償でご提供、3ヶ月後の再診時の費用割引あり
問い合わせ先
research-CE*vsec.jp *は@に置き換えて下さい
担当:[内科]福島 建次郎
早期慢性腎臓病療法食
猫の早期慢性腎臓病の猫に対する
療法食の比較試験
概要
早期慢性腎臓病(IRISステージ1~2)の猫を対象に、特別に設計された腎臓病用療法食の有効性および安全性を評価します。
背景・目的
慢性腎臓病(CKD)は猫に高頻度に認められる疾患であり、特に高齢猫において発症リスクが増加します。実際、15歳以上の猫の約8割が腎機能に何らかの異常を抱えていると報告されています。CKDは進行性であり、現時点では根治させることはできません。そのため、食事療法によって進行を遅らせ、QOL(生活の質)を維持することがきわめて重要です。
こうした背景から、本試験では早期慢性腎臓病(IRISステージ1〜2)の猫を対象に、特別に設計された腎臓病療法食の効果を検証します。3種類の療法食を比較することで、体重や筋肉量を適切に維持しながら腎機能の保全を目指し、QOLと生存期間をより長期にわたり延ばすための栄養学的アプローチを明らかにすることを目的としています。
対象
- 年齢2〜16歳
- 健康状態が良好(BCS ≧2/5)
-
以下のうち1つ以上を満たす
- SDMA >14 μg/dL
- Cre >1.6 mg/dL
- USG <1.035
- UPC >0.4
- 腎臓に形態異常がある
除外基準
- IRIS stage 3以上のCKD
- CKD以外の全身性疾患がある
- 手術の予定がある
- 妊娠している

内容
- 本試験は 無作為化二重盲検試験 として実施されます。猫は無作為に(ランダムに)A・B・C のいずれかの試験食群に割り当てられます。試験食はいずれも、欧州獣医栄養学専門医 Dr. Marco Fantinati(ファルミナペットフーズ・ジャパン株式会社)が設計したもので、安全性が確認され、総合栄養食としての基準を満たしたウェットフードです。
- この試験にご参加いただく場合、試験食は1年間、無料でご提供いたします。
- 試験期間は 1年間 です。初診・3か月・6か月・9か月・12か月にご来院いただき、診察と検査を行います。検査内容は身体検査、血圧測定、血液検査、尿検査です。ご希望があれば、初診時に超音波検査(実費)を追加することも可能です。また、毎月ご自宅で体調に関するアンケートにご記入いただき、健康状態を記録していただきます。
- 本研究への参加は完全に任意です。試験途中であっても、ご家族のご希望により いつでも中止することが可能です。
参加に当たってのご注意
- 試験期間中は、割り当てられた試験食のみを与えていただき、間食や他のフード・サプリメントの使用はご遠慮ください。
- 診察や血液検査など、通常診療にかかる検査費用はご家族のご負担となりますので、あらかじめご了承ください。
-
試験途中であっても、以下のような場合には参加を中止していただきます。
- CKD が進行した場合
- 副作用を認めた場合
- 他に治療を必要とする病気やけがを認めた場合
- 試験食以外のフード・間食やサプリメントを与えた場合
- 2回以上連続して試験食を食べなかった場合
問い合わせ先
research-ckd*vsec.jp *は@に置き換えて下さい
担当:[内科]福島 建次郎/井上 亜希子
尿路上皮癌
犬の尿路上皮癌に対する
放射線治療とがん免疫療法の有効性に
関する臨床試験
概要
犬の尿路上皮癌(UCC)は局所浸潤性および転移率が高く、長期制御が困難な悪性腫瘍です。本試験では、局所制御を目的とした放射線治療と、免疫抑制環境を解除する抗CCR4抗体(モガムリズマブ)を併用し、その有効性および安全性を前向きに評価します。本研究は東京大学獣医臨床病理学研究室との共同研究として実施されます。
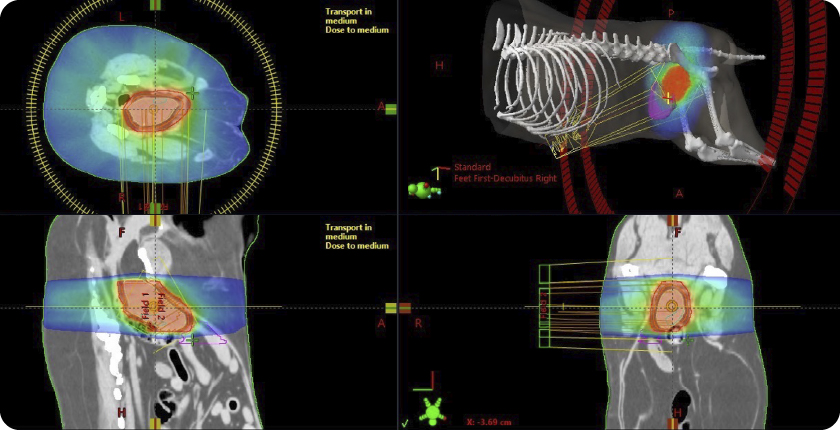
背景・目的
犬の尿路上皮癌に対する治療は、外科切除、放射線治療、NSAIDsや抗がん剤などの内科療法が主軸となっています。しかし、診断時にすでに局所浸潤や転移を伴う症例が多く、完全切除が可能な症例は限られます。放射線治療は局所制御および排尿症状の改善に有効ですが、全身病変への影響は限定的です。一方、全身療法単独では局所制御が十分でない症例も存在します。
近年、腫瘍微小環境における免疫抑制の関与が注目されています。抗CCR4抗体(モガムリズマブ)は、制御性T細胞(Treg)を抑制することで抗腫瘍免疫を増強する分子標的薬であり、犬の尿路上皮癌においても単剤での有効性と忍容性が報告されています。
放射線治療は腫瘍抗原放出や免疫原性細胞死を誘導することが知られており、免疫療法との併用により相乗効果が期待されます。しかし、犬UCCにおいて両者の併用療法を前向きに検証した報告はありません。
本試験の目的は、放射線治療と抗CCR4抗体併用療法の①客観的奏効率、②無増悪期間(PFS)、③全生存期間(OS)、④有害事象(VCOG-CTCAE)を評価し、その臨床的有用性および安全性を明らかにすることです。
対象
下部(膀胱、尿道)尿路上皮癌と診断されている(疑いでも構いません)
除外基準
- すでに抗がん剤、放射線治療、外科手術を行っている
- 水尿管・水腎症あるいは尿道閉塞がある
- IRIS stage 3〜4の慢性腎臓病がある
- 全身状態が悪く、2〜3ヶ月以内に斃死する可能性がある
内容
- 本試験は無作為化二重盲検試験です。本試験への参加をご希望された場合は、無作為(ランダム)に試験群とプラセボ群に3:2の割合で分けられます。
- 試験群は試験薬であるモガムリズマブ(商品名:ポテリジオ®)、プラセボ群はプラセボ薬である生理食塩水を試験開始日より4週間ごとに計3回静脈点滴で投与します。投与時には血液検査・X線検査・超音波検査を実施し、放射線治療と内科療法の併用治療の有効性と副作用を確認します。
- ご自宅では犬の尿路上皮癌に対して一般的に使用されるNSAIDsであるフィロコキシブ(商品名:プレビコックス®)を1日1回、毎日服用していただきます。
- 試験薬あるいはプラセボ薬を初回投与した1週間後より放射線治療を3週間かけて実施します。
- 初回投与から12週間後に血液検査・X線検査・超音波検査を実施し、放射線治療と内科療法の併用治療の有効性と副作用の最終的な確認を行います。この12週間を試験期間とします。
- 試験期間後は、フィロコキシブの内服を継続し、1~2ヵ月ごとの定期健診を行います。
- 試験期間内に腫瘍の進行や重い副作用がみられた場合、獣医師の判断で臨床試験を中止することがあります。
- ご家族様が臨床試験の中断をご希望された場合にはその時点で臨床試験を終了し、通常の治療に移行します。中断のお申し出によりご家族様が不利益をこうむることはありません。
- この臨床試験はVSEC臨床研究倫理委員会の承認を受けています。
問い合わせ先
research-ucd*vsec.jp *は@に置き換えて下さい
担当:[放射線腫瘍科]塩満 啓二郎/吉川 陽人 [内科]井上 亜希子